آخرین مطالب
امکانات وب
انتقال انرژی
انرژی، قابلیت انجام کار است. انرژیهای یک سیستم، شامل انرژی پتانسیل، درونی و جنبشی هستند. تغییرات انرژی یک سیستم را میتوان به صورت زیر بیان کرد:
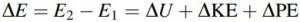
در این معادله تغییرات انرژی پتانسیل، جنبشی و درونی، به ترتیب برابر هستند با:
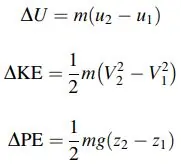
در اکثر مسائل مهندسی، تغییرات انرژی جنبشی و پتانسیل وجود ندارند. با این فرض میتوان تغییرات انرژی سیستم را به صورت زیر بیان کرد:
![]()
در بسیاری از متون علمی، پارامتری که مورد بررسی قرار میگیرد انرژی بر واحد جرم است که معادل است با:
![]()
انتقال جرم
هر جرمی که به درون سیستمی وارد میشود، حامل انرژی است. بنابراین در هنگام وارد شدن تودهای از جرم به یک سیستم، انرژی آن افزایش و در هنگام خارج شدن از آن، انرژی سیستم کاهش مییابد. زمانی که جرمی با نرخ m به یک سیستم وارد میشود، نرخ انرژی وارد شده به آن برابر است با:
![]()
در این معادله h=u+pv است و pv، کار جریان نامیده میشود. در ادامه در مورد اجزا تشکیل دهنده این معادله بیشتر صحبت خواهیم کرد.
انتقال حرارت
«جیمز ژول» (James Joul)، برای اولین بار و با استفاده از آزمایش، نشان داد که انرژی، این قابلیت را دارد که به شکلهای مختلفی تبدیل شود. گرما، شکلی از انرژی است و انتقال حرارت نیز زمانی اتفاق میافتد که در یک محیط جامد و یا سیال، اختلاف دمایی وجود داشته باشد. واحد انتقال حرارت نیز همانند انرژی است. انتقال حرارت با Q نشان داده میشود و این مقدار بر واحد جرم را با q نمایش میدهند. میزان انتقال حرارت صورت گرفته بر واحد زمان را نرخ انتقال حرارت مینامند. به فرآیندی که در آن هیچ انتقال حرارتی اتفاق نمیافتد، «آدیاباتیک» میگویند.
کار
انرژی که به دلیل اختلاف فشار و یا نیرو به سیستم وارد و یا از آن خارج میشود را کار مینماند و آن را با W نشان میدهند. کار شفت، انرژی مکانیکی است که محور دستگاههایی همچون پمپ، توربین و یا کمپرسور را به چرخش در میآورد. به میزان انرژی انتقال یافته بر واحد زمان، توان گفته میشود. میتوان جهت جریان ورودی و یا خروجی از سیستم را در معادلات مربوطه با in و out نشان داد. در شکل زیر میتوانید شماتیکی از مبادله انواع انرژی با سیستم را مشاهده کنید.
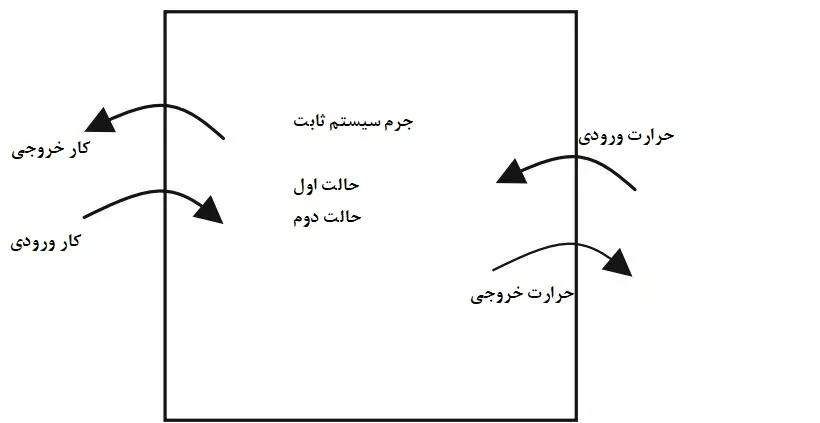
مبادله حرارت و کار با سیستمی با جرم ثابت که از حالت اول به حالت دوم، تغییر میکند.
قانون اول ترمودینامیک
قانون اول ترمودینامیک، بر مبنای آزمایشات صورت گرفته، بیان میکند که انرژی نه میتواند به وجود بیاید و نه از بین برود بلکه از شکلی به شکل دیگر تبدیل میشود. بر مبنای این قانون، تغییرات انرژی کل یک سیستم را میتوان به صورت زیر بیان کرد:
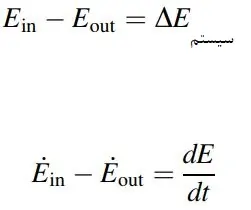
برای سیستم بستهای که تحت یک فرآیند از حالت 1 به 2 تغییر میکند، میتوان نوشت:
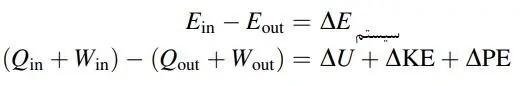
با فرض ثابت بودن انرژی پتانسیل و جنبشی، رابطه زیر برقرار است:
![]()
حال سیستمی را در نظر بگیرید که یک فرآیند پایا را تجربه میکند. در چنین فرآیندی، انرژی و جرم کلی سیستم ثابت است؛ بنابراین قانون اول ترمودینامیک، برای این سیستم به صورت زیر است:
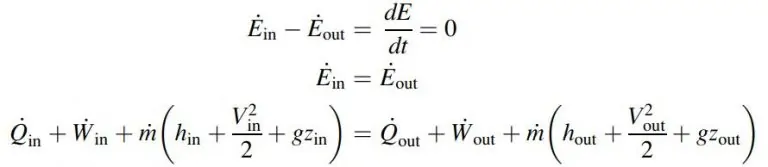
با صرف نظر کردن از تغییرات انرژی جنبشی و پتانسیل میتوان نوشت:
به عنوان مثال، فرآیند پر و یا خالی کردن یک مخزن از گاز را در نظر بگیرید. توجه داشته باشید که در اکثر فرآیندهای ترمودینامیکی، از فرض گاز ایدهآل استفاده میشود. چنین فرآیندی گذرا است؛ بنابراین با در نظر گرفتن جریان به صورت یکنواخت، معادله تعادل انرژی و جرم، به صورت زیر است:
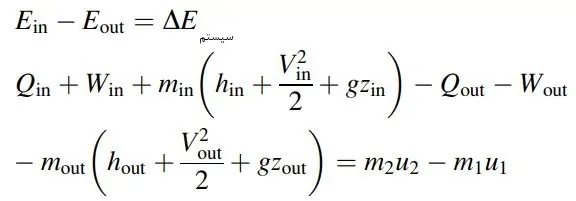
شیمی...
برچسب : نویسنده : amin2051 بازدید : 75
